根据国际癌症研究机构(IARC)的最新估计,2022年全球报告了近2000万新发癌症病例和970万癌症相关死亡病例。结直肠癌的发病率排名第三,死亡率排名第二,构成了重大的健康负担和全球公共卫生挑战。结直肠癌的临床治疗通常采用放疗、化疗、分子靶向药物和手术切除相结合的多模式治疗方法;然而,大多数患者在综合治疗后出现复发。因此,亟需开发新型有效的用于结直肠癌的治疗方法。
免疫疗法是癌症治疗中的一种创新策略,旨在激活和调节患者的免疫系统,以特异性识别和消除癌细胞,具有实现治愈效果的潜力。各种癌症治疗策略,包括免疫刺激细胞因子、检查点抑制剂、嵌合抗原受体(CAR)T细胞、癌症疫苗和溶瘤病毒(OV)免疫疗法,已被提出用以激活免疫系统。溶瘤病毒(OV)疗法是一种新型的多功能癌症治疗方法,能够选择性杀死肿瘤细胞,同时激活全身免疫反应。其中,溶瘤腺病毒(ADV)因其作为基因治疗载体的临床试验数量不断增加而成为最广泛使用的OV之一。然而,自我复制受限、宿主抗病毒免疫及引发负向免疫反馈等问题,导致ADV在临床应用中被局限。借助ADV高水平的基因表达和成熟的生产技术,将其改造为新型治疗性腺病毒仍然是ADV研究的焦点。因此,通过基因改造以构建表达各种蛋白质的新型治疗性溶瘤ADV来克服ADV治疗的局限性,提高其抗肿瘤疗是有前景且可行的方法。
在最新的研究中,必赢76net线路江春平/吴俊华团队构建重组ADV,展示其促进肿瘤微环境M1极化,逆转效应记忆/效应CD8+T细胞浸润不足,增强溶瘤腺病毒的抗结直肠癌疗效,具有潜在的临床治疗前景,为推进ADV疗法治疗结直肠癌提供新的见解。
这项研究首先利用MC38和CT26小鼠皮下肿瘤模型评估了ADV的治疗效果,证明了ADV显著抑制肿瘤生长,并延长小鼠生存时间,但是流式细胞术分析显示,ADV治疗引发肿瘤负免疫反馈,表现为效应记忆/效应CD8+T细胞(TEM/TE)浸润显著减少和M2巨噬细胞浸润增加(图1)。
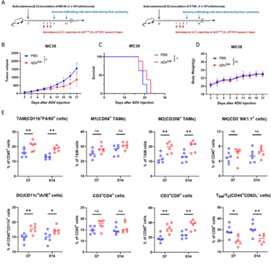
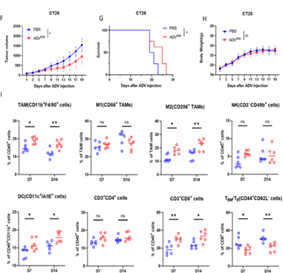
图1. ADV 对皮下结直肠癌模型小鼠的治疗效果及其对肿瘤微环境的影响。
有研究表明,中性粒细胞弹性蛋白酶(NE)和与NE结构相似的猪胰腺弹性蛋白酶(PPE)对多种肿瘤细胞系表现出强烈的选择性细胞毒性,并显著增加肿瘤组织中的TEM/TE浸润。研究团队对癌症基因组图谱(TCGA)数据库分析显示,负责编码NE的ELANE基因在正常组织中的表达高于肿瘤组织,且ELANE高表达的结直肠癌患者预后更好。鉴于此,研究团队构建了表达NE和PPE的溶瘤腺病毒,命名为ADVNE和ADVPPE。通过体外细胞实验证明ADVNE或ADVPPE在不影响非肿瘤细胞的情况下,显著诱导结直肠癌细胞焦亡并增加HMGB1的释放(图2)。随后,在小鼠结直肠癌模型中对ADVNE或ADVPPE的抗肿瘤功效进行验证,结果显示,相较于ADV治疗组,ADVNE或ADVPPE治疗组显著抑制肿瘤生长,延长小鼠生存期,并出现肿瘤完全缓解的小鼠。对治愈的小鼠重新接种MC38细胞时,形成持久免疫力(图3)。体内体外实验共同证明了ADVNE或ADVPPE的抗结直肠癌效果。
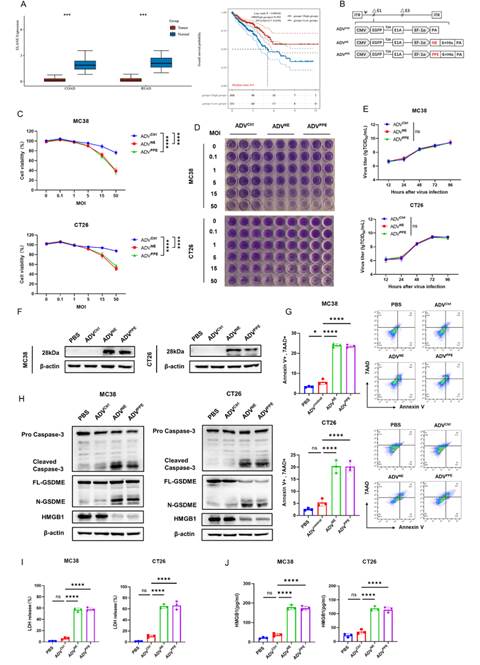
图2 ADVNE 和 ADVPPE 的构建和表征及其体外抗肿瘤机制的研究
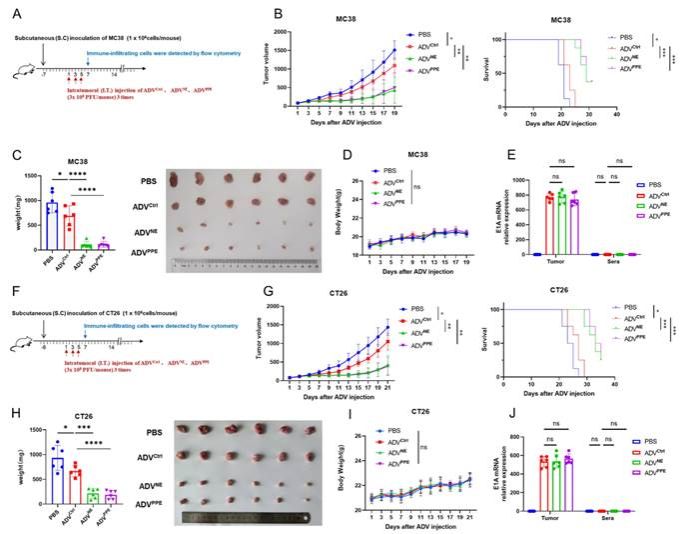
图3 重组溶瘤腺病毒 ADVNE 和 ADVPPE 在结直肠癌小鼠模型中的抗肿瘤作用
研究团队紧接着对ADVNE或ADVPPE的抗肿瘤功效的作用机制展开研究。通过免疫细胞耗竭等实验发现,ADVNE或ADVPPE增强的抗肿瘤效果依赖于巨噬细胞和CD8+T细胞的存在。具体表现为重组ADV表达的NE和PPE促进TAM向M1表型极化,从而增加TME中CD8+T细胞和TEM/TE的浸润,增强ADV的抗肿瘤疗效(图4)。
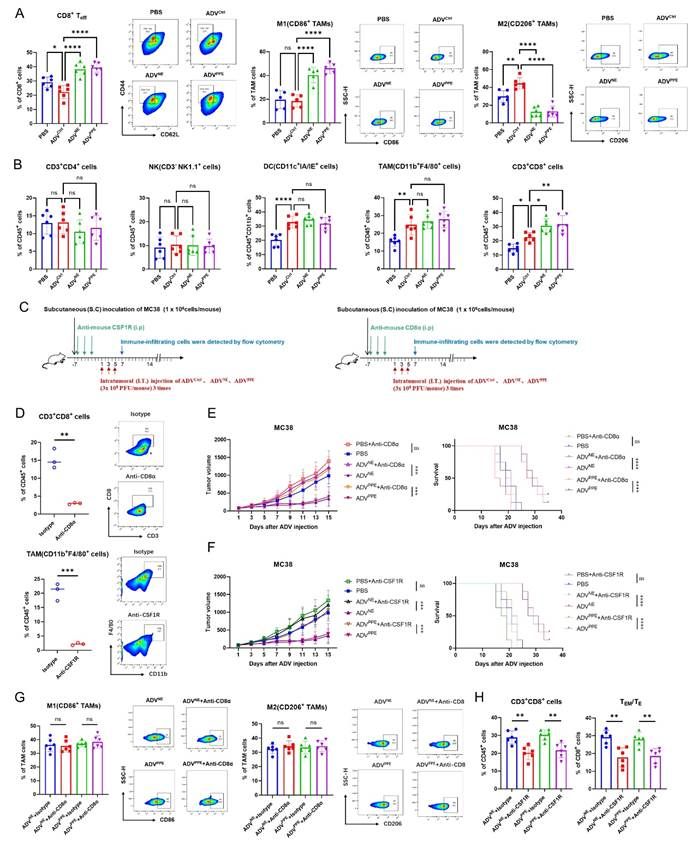
图4 ADVNE 和 ADVPPE 对巨噬细胞 M1 极化和 TEM/TE 浸润的影响
紧接着,团队借助体外细胞培养证明,重组病毒处理的肿瘤细胞培养基显著促进了骨髓来源的巨噬细胞(BMDMs)的M1极化,抑制了M2极化。有报告表明,HMGB1可以诱导巨噬细胞M1极化。本研究观察到重组腺病毒处理的结直肠癌细胞释放到培养基中的HMGB1显著增加,而HMGB1缺陷的肿瘤细胞的培养基无法诱导BMDMs的M1极化。这进一步揭示了ADVNE和ADVPPE表达的NE或PPE诱导肿瘤细胞释放HMGB1,导致了肿瘤微环境中巨噬细胞的M1极化(图5)。
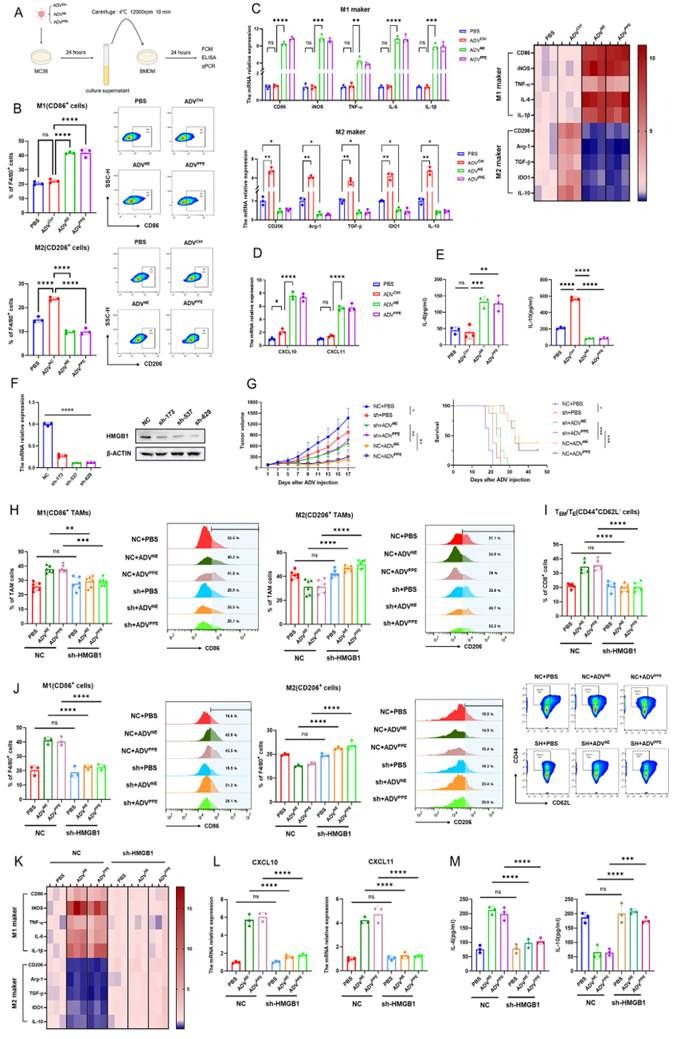
图5 ADVNE 或 ADVPPE 处理的肿瘤细胞释放 HMGB1 对巨噬细胞极化和 TEM/TE 浸润的影响
利用体内和体外实验探究HMGB1与巨噬细胞M1极化之间的关系,进一步揭示了ADVNE或ADVPPE处理的肿瘤细胞释放的HMGB1通过与巨噬细胞上的TLR4受体结合,激活MyD88-NFκB-NLRP3(ASC)通路,进而诱导巨噬细胞M1极化(图6)。
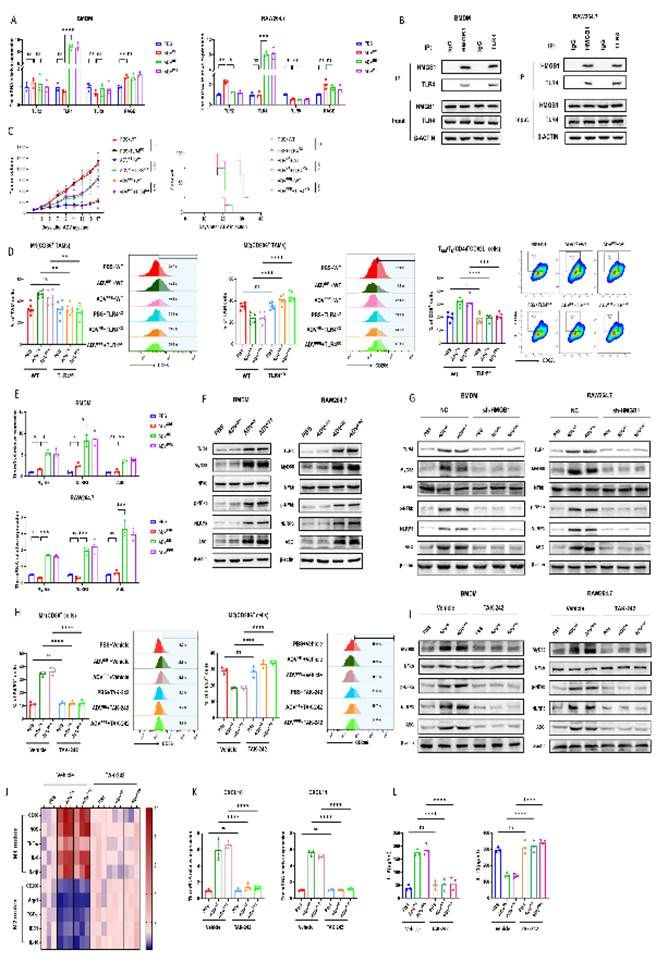
图6 用 ADVNE 或 ADVPPE 处理的肿瘤细胞释放的 HMGB1 与通过 TLR4‒MyD88‒NFκB‒NLRP3 (ASC) 通路诱导 M1 巨噬细胞极化之间的关系
最后,研究团队使用人源化HCT116皮下瘤模型确认ADVNE和ADVPPE的临床转化潜力。结果显示,与ADV治疗组相比,ADVNE或ADVPPE在人源化HCT116模型中表现出显著更强的抗肿瘤免疫治疗效果。此外使用免疫正常的C57BL/6小鼠模拟生理条件下的自然抗病毒免疫反应,评估重组病毒的安全性,H&E染色显示,重组病毒治疗对小鼠器官没有明显损伤(图7)。
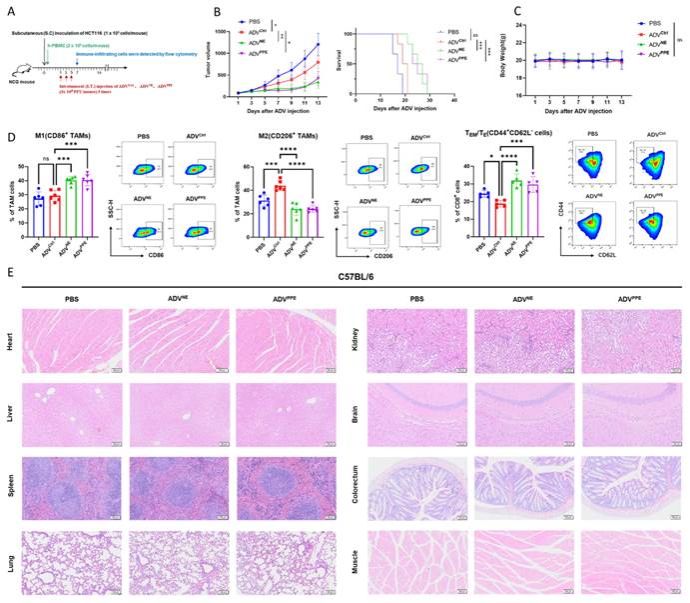
图7 ADVNE 和 ADVPPE 在人源化 CDX 模型中的抗肿瘤免疫治疗作用,肿瘤微环境中特异性免疫细胞的表征,以及初步安全性观察。
本研究设计构建了具有增强抗肿瘤效果的新型重组溶瘤腺病毒:ADVNE和ADVPPE,并证明两者通过诱导结直肠癌细胞发生焦亡且伴随HMGB1释放,后者通过与巨噬细胞上的TLR4受体结合,激活MyD88-NFκB-NLRP3(ASC)通路,进而诱导巨噬细胞M1极化,从而增加TEM/TE细胞浸润并增强抗肿瘤疗效。同时证实了它们的临床转化潜力,为溶瘤腺病毒治疗结直肠癌提供了新的有效策略。
近日,必赢76net线路江春平教授/吴俊华教授团队Journal of Experimental & Clinical Cancer Research(IF:11.4,中科院一区,TOP期刊)上发表了题为“Viral expression of NE/PPE enhances anti-colorectal cancer efficacy of oncolytic adenovirus by promoting TAM M1 polarization to reverse insufficient effector memory/effector CD8+ T cell infiltration”的研究论文。必赢76net线路博士生王硕,必赢76net线路附属鼓楼医院博士后孔令凯等人为该研究论文的共同第一作者。必赢76net线路江春平教授、吴俊华教授和顾晓松院士为该论文的共同通讯作者。
该研究得到了国家自然科学基金(编号81972888, 82272819)、省重点研发计划(编号BE2022840)和省实验室项目(编号SYS202202、JNL-2025008B、JNL-2025009B、JNL-2025011B、JNL-2025010B、JNL2025012B和JNL-2023017D)的资助。
原文链接: https://doi.org/10.1186/s13046-025-03358-y
